Úvod
Spalovaní dřeva a dřevěného odpadu v kotli na ohřev vody může být nahrazeno spalováním slámy nebo jiných zbytků rostlinné zemědělské výroby. I v živočišné výrobě vzniká odpad v podobě kejdy a chlévské mrvy, který lze ve speciálních kontejnerech, za pomocí bakterií rozkládat na plynné produkty. Takové plynné produkty lze dokonce spalovat přímo ve spalovacích motorech nebo v plynových kotlích. Jako palivo pro spalovací motory se používá i bionafta – nafta obsahující uhlovodíky získávané úpravou biomasy (například lisování plodů řepky olejné). Těmto a podobným způsobům využití biomasy se říká energetické využití biomasy.
Biomasa je důležitý lokální zdroj energie, protože ji lze využít pouze v místě nebo nedaleko místa produkce. To je dáno vysokými přepravními náklady biomasy, které jsou způsobené její nízkým měrným energetickým obsahem. Výkon energetického zařízení jehož palivem je biomasa, tedy závisí i na velikosti spádové plochy, na které může být biomasa produkována, Obrázek 239.

Rostlinná biomasa
Prvkové složení rostlin
Rostlinná biomasa neboli fytomasa se skládá z organické hmoty, vody a nízkého obsahu nehořlavých minerálů tzv. popelovin. Organická hmota je tvořená organickými prvky C, H, O, N, viz Tabulka 240. Ve fytomase lze nalézt i neorganické hořlavé prvky nejčastěji S, Ch. Uvedené prvky jsou vázány v hmotě rostlin ve sloučeninách.
| C | H | O | N | S | A | W | |
| σ | 44 | 4 | 34,7 | 0,9 | 0,4 | 4 | 12 |
Fytomasa by v tak velkém množství síru a chlór neměla obsahovat. Tyto prvky se do biomasy dostávají ze vzduchu, do kterého se dostávají z části díky lidské činnosti (spalování fosilních paliv) a z části při přírodních "katastrofách" (výbuch sopky...).
kterého se dostávají z části díky lidské činnosti (spalování fosilních paliv) a z části při přírodních "katastrofách" (výbuch sopky...).
Popelovin je v rostlinné biomase velice málo od 0 % až po několik málo procent, jsou to minerály pocházející z půdy a rostliny je potřebují ke svému růstu. Proto při spalování biomasy vzniká tak málo popela. Popel navíc může obsahovat nespalitelné zbytky hrubých nečistot, které byly do kotle přineseny spolu s palivem (hlína, prach...).
Fotosyntéza a růst fytomasy
Uhlík získává fytomasa ze vzduchu, zbylé prvky a vodu z půdy. Potřebné procesy probíhající v rostlině (doprava potřebných sloučenin, stavba a regenerace žívé hmoty) jsou energeticky, a z velké části i prvkově, hrazeny respirací glukózy C6H12O6 (oxidace glukózy vzdušným kyslíkem při vylučování molekuly CO2 – porovnejte s dýcháním), která vzniká v listech při jejich oslunění procesem zvaným fotosyntéza.
Fotosyntéza je proces, při kterém se plynná složka vzduchu CO2 rozkládá, respektive přetváří v molekuly glukózy pomocí sluneční energie. Fotosyntéza probíhá za přítomnosti chlorofylu, který je katalyzátorem probíhajících chemických reakcí, Obrázek 241.

Při fotosyntéze pigmenty chlorofylu zachytávají světlo pomocí něhož rozkládají molekuly vody H2O na kyslík a ionty vodíku H+, tomuto ději se říká fotolýza (podobný princip jako u palivového článku). Elektrická energie (putující elektron) a ionty vodíku jsou využity k tvorbě organických sloučenin. Odpadem je čistý kyslík uvolňovaný do atmosféry (ve formě O2 jehož jednotlivé atomy jsou původem z rozkladu H2O a nikoliv CO2 [12], [13]). Tento popis fotosyntézy lze zapsat Rovnicí 561, nicméně se jedná o značné zjednodušení se zaměřením se pouze na počáteční a výsledné produkty.
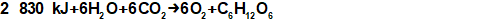
Účinnost fotosyntézy je až 3 % (roční průměr kontinentální biomasy je asi 0,33 % a oceánské jen 0,1 % [13] – vztaženo k celkové osluněné ploše).
Energetické výnosy fytomasy
Biomasa jako palivo má své energetické parametry. Těmi nejdůležitějšími ukazateli v tomto směru je její výhřevnost, případně spalné teplo při hoření. Tyto parametry jsou dány druhem biomasy. Chceme-li pěstovat například fytomasu pro energetické účely, pak nás musí zajímat kolik využitelné energie případně hmoty či objemu jsme schopni sklidit ve fytomase z jednotky plochy – taková veličina se nazývá výnos., viz Tabulka 242. Například v případě obilné slámy lze získat z jednoho hektaru kolem 16 000 kWh – pro představu roční spotřeba tepla (teplá voda+topení) rodinného domku (nezateplený) může převyšovat 25 000 kWh.
| Q | x | V | ||
| 1 | sláma 1 | 14 | 15 | 3-5 |
| 2 | sláma 2 | 13,5 | 17-18 | 4-6 |
| 3 | seno 1 | 12 | 15 | 2-8 |
| 4 | seno 2 | 12 | 15 | 2-4 |
| 5 | jiné jednoleté | 14,5 | 18 | 15-20 |
| 6 | dřeviny | 12 | 25-30 | 8-12 |
| 7 | energo rostliny | 14,5 | 18 | 15-25 |
K pěstování fytomasy nelze přistupovat čistě energeticky, protože její existence má i jiné efekty. Rostliny vyrábí kyslík, jsou potravou apod. Navíc přímo i nepřímo ovlivňují klima či počasí, například velké množství vody se pomocí rostlin odpaří, a tím ochlazuje okolí, a naopak tato energie se vrací v noci jako rosa (udržování teploty i v noci). Obvykle zemědělec nemůže pěstovat jen fytomasu s nejvyšším en. výnosem, ale je omezen i půdou, problémy monokultur, případně legislativními podmínkami a pod.
Klasifikace energetických transformací biomasy
Energii obsaženou v biomase lze získat nejen jejím spálením ve formě tepla za vzniku spalin a tuhých zbytků (popel), ale také dalšími cestami. Jejich základní rozdělení je podle toho, co je hlavním hybatelem rozkladu sloučenin v biomase obsažených, kterým může být buď teplota, bakterie nebo mechanická destrukce.
hlavním hybatelem rozkladu sloučenin v biomase obsažených, kterým může být buď teplota, bakterie nebo mechanická destrukce.
Přirozený rozpad biomasy
Jedná se o rozpad způsobený reakcí organických sloučenin s kyslíkem podporované tepelným pohybem atomárních struktur často za vzniku nových sloučenin. Organické sloučeniny v kyslíkovém prostředí podléhají rozkladu a dokud je organismus živý, tak tento rozklad kompenzuje regeneračními procesy. Nicméně mrtvý organismus, například odumřelá větev stromu, se časem rozpadá vlivem interakce se vzdušným kyslíkem, až po několika letech zcela zmizí, a zbudou po ní jen složky nepodléhající při daných podmínkách oxidaci (různé anorganické složky, minerály...). Za ideálních podmínek se biomasa rozpadá na CO2 a H2O. Při tomto rozkladu se uvolňuje energie ve formě tepla. Rychlost rozkladu významně závisí na teplotě okolí (roste přibližně 2 až 3x při zvýšení o 10 °C), na vzdušnosti okolí a klimatických podmínkách.
Biomasa se rozkládá i nezávisle na kyslíkové atmosféře (tzv. anaerobní děj). Uhlík reaguje s kyslíkem a vodíkem v biomase a vytváří CO, respektive CH4. K rozkladu bez přítomnosti vzdušného kyslíku, ale významně dochází pouze při vyšších než pokojových teplotách nebo za přítomnosti bakterií. Popišme si ale rychlejší termochemické transformace biomasy, které lze v reálném čase využít k energetickým účelům.
Spalování biomasy
Spalování je vysokoteplotní a současně nejrozšířenější způsob využití biomasy, kdy se využívá slučovací entalpie uvolněná při hoření k rozpadu organických sloučenin a k ohřevu okolí. Produktem jsou spaliny a popel.
Při spalování hoří pevný uhlík, případně vodík obsažený v palivu, i unikající plynné látky. Vzduch je pokud možno přiváděn ve všech částech spalovacího prostoru (topeniště) a jeho celkové množství je vyšší než odpovídá stechiometrickému spalování – viz podkapitola Hoření jako chemický proces. Pro hoření biomasy je charakteristická vysoká teplota. Proces hoření má v tomto článku samostatnou kapitolu Hoření biomasy, s. 8
Zplyňování biomasy
Při zplyňování (nedokonalé hoření) hoří uhlík obsažený v palivu v jiné části spalovacího zařízení než unikající plynné produkty (ty není nutné ihned spalovat, ale mohou se odvádět a využívat mimo zplyňovací zařízení). Takže mimo popela je produktem ještě hořlavý plyn zvaný generátorový, zuhelnatělé zbytky (hořlavé) a dehtový olej. Aby tyto produkty vznikly, musí hoření probíhat nedokonale s malým množstvím kyslíku, tzv. podstechiometrické spalování.
a dehtový olej. Aby tyto produkty vznikly, musí hoření probíhat nedokonale s malým množstvím kyslíku, tzv. podstechiometrické spalování.
Na Obrázku 244 je řez zplyňovacím kotlem na kusové dřevo s pevným ložem. Do horní části spalovací komory je přiváděno takové množství vzduchu, aby probíhalo pouze podstechiometrické hoření. Zde hoří především uhlík na CO (typický produkt nedokonalého spalování) a CO2. Přitom dochází k uvolnění dalších hořlavých plynů z termického rozpadu dřeva. Vzniklé spaliny a plyn jsou vedeny do dolní části spalovací komory, kam je také přiváděn další vzduch (sekundární), který hoří s CO a dalšími plyny. Vzniklými horkými spalinami se ohřívá voda. Dále se uvolňují dehtové látky a odpadní fenolové vody [6]. Zplyňování v zařízení s pevným ložem probíhá při atmosférickém tlaku.
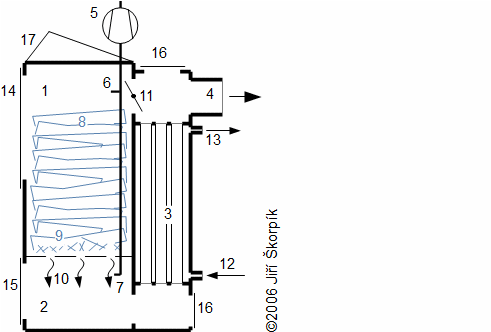
Existují i jiné způsoby zplyňování [3], ale podstata zůstává stejná. Například zplyňování při tlaku až 2,5 MPa a teplotách 850 °C až 1000 °C. Toto zplynění probíhá pomocí fluidní vrstvy ve fluidních generátorech. Při těchto teplotách dochází k rozkladu dehtů, fenolů i mastných kyselin na spalitelné plyny. K vysokotlakému zplyňování je zpravidla přistoupeno kvůli tomu, aby generátorový plyn byl co nejčistší (typické objemové složení 8 až 10 % CO, 4 až 8 % CH4, 8 až 12 % H2, 11 až 8 % CO2, 7 až 10 % H2O, zbytek je N2, potom je výhřevnost vyrobeného plynu 2,5 až 8 MJ·m-3n, ale existují i způsoby zplyňování, u kterých je podíl dusíku mnohem menší a výhřevnost až 14 MJ·m3n). Tento plyn není dále spalován, ale je zbavován tuhých částic (filtry) a chlazen. Výsledný plyn je potom dále využit třeba jako palivo do spalovacího motoru kogenerační jednotky, nebo je možné ještě horký plyn převést pomocí syntézy na kapalné palivo.
Připomenutí doby, kdy auta jezdila na tzv. generátorový plyn, který se vyráběl ze dřeva, dřevěného nebo kamenného uhlí (prostě z čehokoliv co hořelo). Nutnou součástí automobilu byl generátor tohoto plynu, viz obrázek. pic.twitter.com/35akkNZFyw
— Jiří Škorpík (@jiri_skorpik) March 23, 2023
2,5 až 8 MJ·m-3n, ale existují i způsoby zplyňování, u kterých je podíl dusíku mnohem menší a výhřevnost až 14 MJ·m3n). Tento plyn není dále spalován, ale je zbavován tuhých částic (filtry) a chlazen. Výsledný plyn je potom dále využit třeba jako palivo do spalovacího motoru kogenerační jednotky, nebo je možné ještě horký plyn převést pomocí syntézy na kapalné palivo.
Výhodou zplyňování je vysoká účinnost využití energie v palivu a nižší škodlivé emise oproti klasickému spalování. Nevýhodou je složitější zařízení.
Pyrolýza biomasy
Pyrolýza je rozklad biomasy při vysoké teplotě (termický rozklad) bez přívodu vzduchu na pevný hořlavý zbytek (většinou dřevěné uhlí), pyrolýzní plyn a dehtový olej, viz Tabulka 245.
| σ | Q | ||
| 1 | uhlí | 31,8 | 10 216 |
| 2 | živice | 15,8 | 4 689,2 |
| 3 | kyselina octová | 7,08 | 1 009 |
| 4 | metylalkohol | 1,6 | 355,88 |
| 5 | aceton | 0,19 | 62,8 |
| 6 | CO2 | 9,96 | 0 |
| 7 | CO | 3,32 | 339,13 |
| 8 | CH4 | 0,54 | 0 |
| 9 | C2H4 | 0,19 | 0 |
| 10 | různé organické látky | 10,03 | 1 624,5 |
| 11 | voda | 19,49 | 0 |
| 12 | celkem | 100 | 18 296 |
Pyrolýzní proces lze rozdělit podle dosažené teploty na tři části. V oblasti teplot do 200 °C dochází k sušení a tvorbě vodní páry fyzikálním odštěpením vody (oba procesy jsou silně endotermické). V rozmezí teplot 200 až 500 °C následuje oblast tzv. suché destilace. Zde nastává ve značné míře odštěpení bočních řetězců z vysokomolekulárních organických látek a přeměna makromolekulárních struktur na plynné a kapalné organické produkty a pevný uhlík. Ve fázi tvorby plynu v oblasti teplot 500 až 1200 °C jsou produkty vzniklé suchou destilací dále štěpeny a transformovány. Přitom, jak z pevného uhlíku, tak i z kapalných organických látek vznikají stabilní plyny, jako je H2, CO, CO2 a CH4.
V současné době je většina provozovaných pyrolýzních systémů založena na termickém rozkladu biomasy v rotační peci. Pec je ohřívána spalováním části pyrolýzních plynů odebraných z pece. K ohřátí biomasy v peci lze použít i horkého inertního plynu (neobsahující kyslík).
K ohřátí biomasy v peci lze použít i horkého inertního plynu (neobsahující kyslík).
Dřevěné uhlí z pyrolýzního spalování se využívá například ke kování i jako palivo pro grilování. Dřevěné uhlí je totiž čistý uhlík a tedy produktem spalování je pouze CO2, který je bezbarvý a bezpachý, což je při kování i grilování to nejpodstatnější. Pokud by se topilo dřevem, tak vlivem velkého prchavého podílu by oheň dýmil a jeho kouř by obsahoval látky nevhodné pro přípravu jídla a v případě kování by mohlo dojít k prvkové kontaminaci kovaného materiálu.
Alkoholová fermentace biomasy a výroba bioplynu
Jedná se asi o nejznámější biochemickou transformaci, při které se glukóza obsažená v biomase transformuje na alkohol a oxid uhličitý – C6H12O6→2CH3CH2OH+2CO2 katalyzátorem této reakce je enzym (obsažený v kvasinkách), který urychluje přírodní procesy [2, s. 252]. Výsledný produkt CH3CH2OH je Ethanol (alkohol – líh). Toto kvašení probíhá bez přístupu vzduchu (anaerobní fermentace) a místo alkoholu může vznikat i Methanol. Pevným zbytek po alkoholové fermentaci se nazývá vykvašený substrát.
Alkohol je velice dobré palivo a v některých případech může být náhražkou za kapalná fosilní paliva. Takový druh paliva je nejvíce využíván v Brazílii, kde je pro alkoholové kvašení ve velkých objemech používaná cukrová třtina.
Pokračováním alkoholové fermentace při přístupu vzduchu se nazývá aerobní fermentace. Jedná se o transformaci lihu například na kyselinu octovou a vodu přitom se uvolňuje i teplo – CH3CH2OH+O2→CH3COOH+H2O. Je nutná přítomnost octových bakterií. Výsledkem může být např. kyselina octová (ethanová kyselina) a voda (přeměnu alkoholu na octovou kyselinu provází vznik meziproduktů, jako je acetaldehyd [2, s. 256]). Známé je kysnutí vína po jeho otevření apod. Pevný zbytek na konci aerobní fermentace se označuje jako fermentovaný substrát.
Podobný proces jako při alkoholové fermentaci se používá i při biochemické transformaci organických složek zvířecích exkrementů a jiné podobné biomasy. Protože tato biomasa má výrazně jiné složení než fytomasa, tak výsledek je také odlišný, při kterém postrádáme vznik lihu a místo něj vzniká tzv. bioplyn a fermentovaný substrát, proto mluvíme o anaerobní fermentaci. Navíc, oproti alkoholové fermentaci, je nutné udržovat teplotu kolem 35 °C.
Složení bioplynu odpovídá převažující sloučeninové transformaci při anaerobní fermentaci C6H12O6→3CH4 + 3CO2. Typicky bioplyn obsahuje 55 až 60 % CH4, 40 až 45 % CO2 a jiné plyny (1 % sirovodík...) [6]. Problémem při této transformaci je velké množství uvolněné vody a čpavku, což může způsobovat korozi zařízení.
velké množství uvolněné vody a čpavku, což může způsobovat korozi zařízení.
Tento způsob zplyňování biomasy se často používá v bioplynových stanicích se spalovacími motory, pro které je bioplyn palivem. K anaerobní fermentaci na bioplynových stanicích se používají velké nádrže (cca 4000 m3), do kterých se dávkuje kejda a obvykle velké množství nařezané kukuřice. Plyn se jímá do rozvodu plynu a rozpadlá biomasa ve formě řídké "kaše" (tzv. fermentovaný substrát) se odčerpává mimo zásobník a většinou se používá jako hnojivo.
Drcení a lisování biomasy
Při drcení a lisování se základní složky biomasy oddělí fyzikální cestou, a kapalná frakce se může případně rafinovat. Tímto procesem vzniká například řepkový olej, který se pomocí rafinace vylisovaného oleje z Řepky olejné může využívat jako tzv. bionafta. Zbylé pevné složky lze například použít jako palivo pro spalovaní.
Hoření biomasy
Biomasa má různou strukturu, ale většinou základní fáze hoření (od termického rozkladu s uvolňováním hořlavých plynů a páry až po hoření uhlíkových zbytků) mají stejnou. V tomto článku je proto uveden detailněji jen popis hoření dřeva, které napovídá o technických potřebách spalovacího zařízení biomasy obecně.
Hoření dřeva
Dřevo (jiný název dendromasa) obsahuje mnoho druhů hořlavin, které mají jinou teplotu hoření, proto při dané teplotě hoří vždy jen určitá část dřeva [7]. Nejdříve je však nutné dřevo zahřát na patřičnou teplotu a odpařit vodu, viz Obrázek 246.
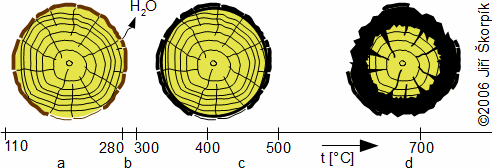
Při zahřívání dřeva do 110 °C se z něho uvolňuje vlhkost (vázaná voda), při vyšších teplotách dochází k pomalému rozkladu, který je provázen uvolňováním tepla. Při těchto teplotách se také uvolňuje CH4 a další uhlíkové řetězce ve formě plynu. Z těchto plynů jen asi 5 až 6 % okamžitě oxiduje. Při teplotách, které odpovídají maximálním výtěžkům plynných produktů (280 až 300 °C) je množství tepla, které se uvolní při rozkladu (oxidace plynů) tak velké, že dřevo je schopné samozahřívání.
Při 290 až 300 °C dochází k největšímu výtěžku plynných produktů, ale na povrchu už se vytváří zuhelnatělná vrstva – pevný uhlík (dřevěné uhlí), a vznik plynných produktů se postupně zastavuje. Teplota uhlí v tomto okamžiku postupně dosahuje 400 až 500 °C. V závislosti na zahřátí horní vrstvy dřeva a jeho přeměny na dřevěné uhlí probíhá zahřátí níže ležící vrstvy dřeva na 300 °C a dochází k jejímu rozkladu. Postupné zvětšování vrstvy uhlíku je provázeno zvyšováním jeho teploty na 700 °C a zmenšováním množství tepla odevzdaného rozkládající se vrstvou dřeva. V důsledku toho se výtěžek plynných produktů zmenšuje a plamen se nevytváří nad celým povrchem hořícího dřeva, ale jen nad trhlinami v povrchu pokrytém uhlíkem. V této fázi je vrstva uhlíku silná 1,5 až 2 cm. Zápalná teplota uhlíku je 690 °C, methanu již 597 °C (vodík snižuje zápalnou teplotu uhlíku), proto dřevo zcela neshoří, dokud teplota dřeva nedosáhne zápalné teploty uhlíku. Například při požáru řídkých dřevěných konstrukcí nemusí být vývin tepla takový, aby shořela celá konstrukce. Z mohutných dřevěných trámů se pouze stanou ohořelé pahýly s vrstvou dřevěného uhlí, ale s relativně nepoškozeným jádrem viz Obrázek 246d a konstrukce se nemusí zřítit.
Výpočet hoření biomasy
Pro konstrukční návrh spalovacího zařízení je nutné znát množství uvolněné energie, množství spáleného kyslíku, respektive vzduchu, výsledné složení spalin a teplotu nechlazeného plamene označovanou tu (tzv. teplota adiabatického hoření – je to maximální teplota spalin, jestliže žádné teplo při hoření není odváděno do okolí).
Množství uvolněné energie spálením 1 kg biomasy se vypočítá z prvkového složení paliva a příslušných chemických reakcí. Například bude-li palivo obsahovat hmotnostně 90 % uhlíku 5 % vodíku a 5 % vody připadají v úvahu chemické reakce, při kterých reaguje uhlík s kyslíkem a vodík s kyslíkem, viz Rovnice 234, s. 10. Jestliže od entalpie, která se při těchto reakcí uvolní odečteme slučovací entalpii původních sloučenin, pak získáme spalné teplo. Takový výpočet je komplikovaný a náročný na rozbor složení biomasy, takže mnohem jednoduší je stanovit spalné teplo a výhřevnost pomocí jednoduchého kalorimetrického experimentu. Navíc prakticky pro většinu známých druhů fytomasy jsou tyto parametry již změřeny, viz Tabulka 242. V mnoha případech je množství uvolněné energie změřeno experimentálně, a spalné teplo či výhřevnost se u jednotlivých paliv většinou už počítat nemusí.
Navíc prakticky pro většinu známých druhů fytomasy jsou tyto parametry již změřeny, viz Tabulka 242. V mnoha případech je množství uvolněné energie změřeno experimentálně, a spalné teplo či výhřevnost se u jednotlivých paliv většinou už počítat nemusí.
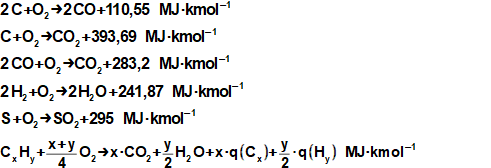
Při vysokoteplotním hoření (nad 1000-1300 °C) může ještě hořet i dusík obsažený v palivu a ve vzduchu, ale tato reakce je nežádoucí, protože sloučeniny NOx patří mezi škodliviny, proto je hoření řízeno tak, aby tato teplota nebyla překročena.
Množství spáleného kyslíku, respektive spotřebu vzduchu při dokonalém hoření se vypočítá z příslušných reakcí stejně tak, jako výsledné složení spalin. Přitom lze vycházet z Tabulky 247, pomocí které lze přepočítat hmotnost daného plynného prvku, či sloučeniny, ze zadaného objemového množství na molové množství.
| M | VM | ||
| 1 | C | 12,01 | – |
| 2 | CO | 28,01 | 22,4 |
| 3 | H2 | 2,016 | 22,43 |
| 4 | N2 | 28,016 | 22,4 |
| 5 | S | 32,06 | – |
| 6 | CH4 | 16,04 | 22,36 |
| 7 | C3H8 | 44,09 | 21,92 |
| 8 | O2 | 32 | 22,39 |
| 9 | Ar | 39,944 | 22,39 |
| 10 | CO2 | 44,01 | 22,26 |
| 11 | SO2 | 64,06 | 21,89 |
| 12 | H2O | 18,016 | 22,4 |
Teplotu nechlazeného plamene lze vypočítat z entalpie spalin. K výpočtu je nutné vědět jaké množství energie (entalpie) do spalovacího procesu sebou přináší jednotlivé vstupní produkty (palivo, vzduch), jaké množství energie se uvolní při spalování (výhřevnost) – o kolik se zvýší po spálení entalpie spalin a závislost celkové entalpie spalin na teplotě, respektive funkci isp=f(t), viz Obrázek 700.
a závislost celkové entalpie spalin na teplotě, respektive funkci isp=f(t), viz Obrázek 700.
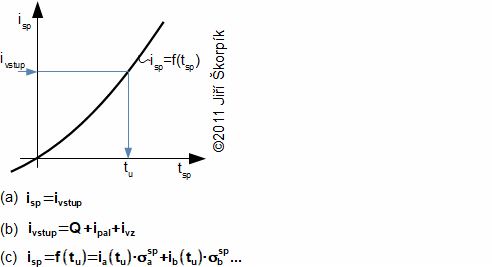
V ideálním případě (dokonalé spalovaní) zvýšení entalpie spalin v důsledku hoření odpovídá výhřevnosti paliva. To znamená, že při hoření se transformuje energie spojená se slučováním molekul pouze na vnitřní tepelnou energii spalin a tlakovou energii. Při spalování paliva ve volném plynném prostředí musí totiž zvětšující se objem spalin vykonat i práci – při svém vzniku spaliny vytlačují okolní plynné prostředí [8, s. 36] (velikost této práce vzhledem k uvolněné energii není velká a ve výpočtu se vynechává).